衰老是细胞分裂的停止和细胞周期的永久退出,是整个生命周期中发生的过程 —— 在胚胎发生、生长和发育、组织重塑以及伤口愈合过程中。衰老细胞的数量在老化过程中增加,并且与机体功能随时间下降以及与年龄有关的疾病的发展有关。这些疾病包括代谢和心血管疾病、神经退行性疾病和癌症。在哺乳动物中,衰老导致多种组织系统以异质方式逐渐出现功能障碍,最终导致死亡。了解衰老如何以及为什么会导致老化过程可能会导致疗法减缓甚至逆转其进展。
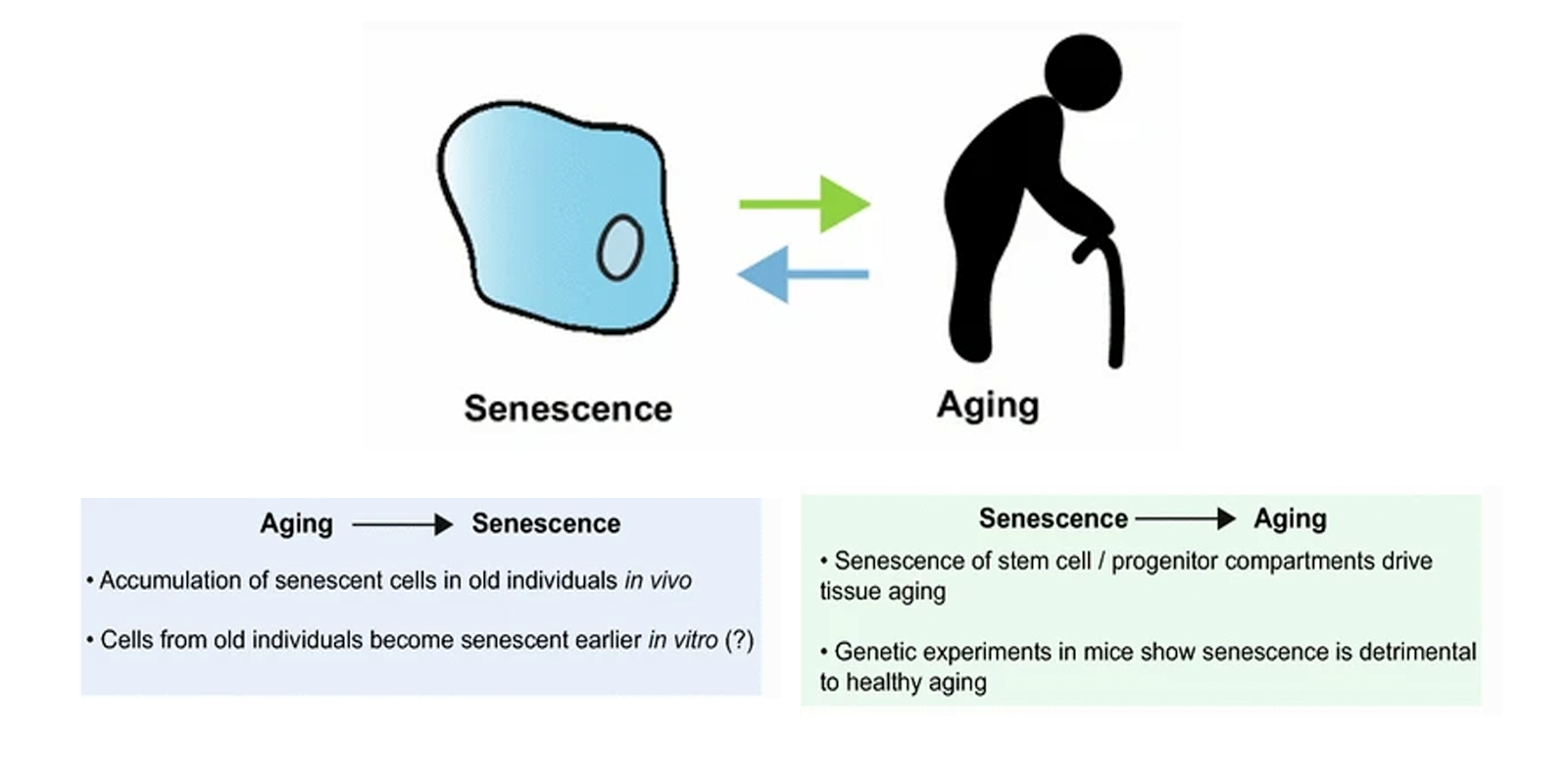
衰老通常是对多种导致细胞 DNA 损伤积累的细胞应激的反应。它也响应端粒缩短而发生。端粒缩短是正常的过程,每轮细胞分裂都会发生,并且是将增殖限制为有限数目的细胞分裂的一种机制。这样,衰老可能已经发展成为防止携带有害遗传突变的细胞繁殖的一种方式。作为对此益处的权衡,衰老及其相关的代谢活性和细胞功能变化参与了衰老过程。
开创性研究已经提供了衰老与老化之间联系的证据,这些研究表明,在动物模型中积极靶向和去除衰老细胞会导致寿命显著延长。实际上,senolytics(一类选择性诱导衰老细胞死亡的化合物)的开发和使用可以延长啮齿动物的寿命并延缓与年龄相关的体力下降。因此,目前正在临床试验中研究 senolytics 对治疗与年龄有关的疾病(例如骨关节炎和慢性肾脏疾病)的疗效。Senolytics 在治疗癌症方面也具有临床潜力,因为化学疗法的负面结果是衰老细胞数量增加,这通常与疲劳和其他有害副作用有关。但是,衰老细胞分泌许多可促进转移的蛋白质,这是其衰老相关的分泌表型(SASP)的结果。因此,将 senolytics 与化学疗法相结合以平衡衰老细胞的正面和负面影响对于治疗某些癌症可能是必要的。
可以通过利用与衰老相关的形态和代谢变化的测定方法来检测老化过程中的衰老细胞。这包括体外衰老细胞的大而扁平的形状和 Lamin B1 表达降低引起的核膜破裂。组蛋白 H2A.X 的磷酸化和衰老相关异染色质病灶(SAHF)的积累是 DNA 损伤的证据,是衰老细胞的常见特征。此外,在衰老过程中观察到调节细胞周期退出的关键蛋白,包括 p53 肿瘤抑制蛋白、细胞周期蛋白依赖性激酶抑制剂(CDKI)p16、 p21 和 p27 以及在 SASP 中(包括促炎性细胞因子、蛋白酶和生长因子。为了研究这些变化,Senescence Marker Antibody Sampler 和 SASP Antibody Sampler Kit 提供了一系列针对常用衰老生物标志物的试剂。
有关细胞衰老、其信号转导通路和用于在您的研究中研究衰老的检测的更多信息,请访问关于衰老信号转导通路的 CST 资源页面。


 沪公网安备31011502018823号
沪公网安备31011502018823号