使用诸如 ChIP-Seq、CUT&RUN 及现在的 CUT&Tag 等方法剖析染色质,已经显著促进我们对疾病机制以及调节表观遗传变化如何可以用来开发新治疗药的理解。使用这三种技术之一生成 DNA 文库后,可以使用诸如 NanoDrop 或 Qubit 系统等平台对文库定量,用诸如 Bioanalyzer 或 TapeStation 系统等仪器做质量控制,并使用下一代测序 (NGS) 加以分析。但是,如果 CUT&Tag DNA 文库浓度或者 Bioanalyzer 或 TapeStation 系统生成的信号低,会发生什么?让我们探索您如何仍然能够成功对您的 DNA 文库测序。
所有 DNA 文库定量方法并不等同
Bioanalyzer 仪或 TapeStation 仪经常用于设立 DNA 和 RNA 样品质量控制。在分析之前,可使用 Thermo Fischer Scientific Nanodrop 仪、Qiagen QIAxpert 系统、Thermo Fisher Scientific Qubit 荧光计定量系统或 PicoGreen 测定法测定文库浓度。然而,已扩增 CUT&Tag DNA 文库的测量产量可能基于所用方法变动。CST 科学家用每种方法测量了同一 DNA 文库,以提供以下 CUT&Tag DNA 文库产量指南。请谨记在心:即使产量低,您仍然可能获得优质 NGS 数据。
| 方法 | 靶标 | 预期浓度 | 建议 |
| NanoDrop 或 QIAxpert 系统 | 组蛋白 | 10–20 ng/µL | 如果您的 DNA 文库浓度 >3 ng/µL,我们建议继续进行 NGS 分析,即使 BioAnalyzer 或 TapeStation 系统上文库 QC 信号微弱或不可见。如果文库浓度 <3 ng/µL,请参阅 CST 疑难解答指南。 |
| 辅助因子或 转录因子 |
5–12 ng/µL | ||
| Qubit 荧光计定量系统或 PicoGreen 测定法 | 组蛋白 | 3–10 ng/µL | 浓度可能太低以致不能在 BioAnalyzer 或 TapeStation 系统上运行。如果您的阳性对照(如三甲基组蛋白 H3 (Lys4) 生成预期的文库产量和/或 Bioanalyzer 峰或 TapeStation 峰,或对 CUT&Tag DNA 文库进行 qPCR QC 生成良好的信噪比,我们建议您仍使用 NGS 分析文库。 |
| 辅助因子或 转录因子 |
<1 ng/µL |
请参阅 CUT&Tag 常见问题 (FAQ) 页面,查看支持性数据和/或了解将不同产量的样品汇集在一起的指导。
DNA 文库质量控制
Bioanalyzer 或 TapeStation 系统为您提供关于样品浓度、片段平均大小范围和样品纯度的信息。当目的靶标(例如转录因子)在细胞中不丰富或仅少数细胞可获得时,来自 Bioanalyzer 仪或 TapeStation 仪的数据可能表明文库产量低。在这些情况下,可能难以知道是否继续进行 NGS,而且很多时候使用 ChIP-seq 或 CUT&RUN DNA 文库的研究人员会选择不继续下去。然而,使用 CUT&Tag 时基线阈值较低,这就引出以下问题:即使来自 Bioanalyzer 或 TapeStation 系统的信号低,我仍可能成功对我的 CUT&Tag DNA 文库测序吗?
即使来自 Bioanalyzer 或 TapeStation 的信号低,CUT&Tag 也可能提供优质 NGS 数据
使用低丰度靶标或少量细胞时,我们建议将阳性对照如 Tri-Methyl-Histone H3 (Lys4) 随您的 DNA 文库一起运行来评估实验步骤成功与否。1 在阳性对照信号高但靶标文库信号低的情况下,仍然可以成功对 CUT&Tag DNA 文库测序,以提供重要的蛋白质-DNA 相互作用数据(图 1)。因此,我们建议即使您在来自 Bioanalyzer 或 TapeStation 系统的谱图中看到极弱峰或甚至看不到可见峰,您仍对 CUT&Tag DNA 文库测序。
从 Bioanalyzer 系统的三个具有低信号的 DNA 文库中获得稳健的 TCF4/TCF7L2 测序数据
.jpg?width=780&height=177&name=23-ETC-03854%20CUT%26Tag%20Bioanalyzer_Blog%20Image1%20(1).jpg)
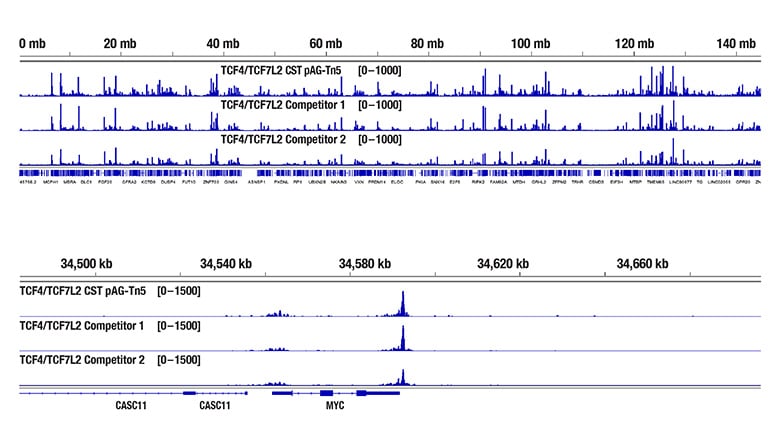
图 1. 以数个加载型 pAG-Tn5 的来源,用 HCT 116 细胞和 TCF4/TCF7L2 (C48H11) Rabbit mAb #2569 进行 CUT&Tag。每种酶的用量基于制造商的建议。使用 CUT&Tag Dual Index Primers 和 PCR Master Mix for Illumina #47415 制备 DNA 文库。图片(上图)显示从 Bioanalyzer 系统对三个 CUT&Tag DNA 文库获得的概况。
对使用 Bioanalyzer 系统分析的相同 DNA 文库测序,并显示 NGS 迹线(下图)。NGS 数据显示等同结合作用遍及第 8 号染色体(上图),包括 TCF4/TCF7L2 的已知靶标基因 MYC(下图)。
qPCR:CUT&Tag DNA 文库的替代性 QC 方法
如果您仍然顾虑对具有 Bioanalyzer 或 TapeStation 系统的低信号结果的 CUT&Tag DNA 文库测序,另一个选择是比照已知的阳性基因座和阴性基因座对 DNA 文库执行 qPCR 作为 NGS 之前的 QC 步骤,以评估染色质片段的富集情况。重要的是指出,应当对 CUT&Tag DNA 文库,而非对文库制备之前的 CUT&Tag DNA 进行 qPCR。CUT&Tag DNA 与文库扩增之前的 qPCR 分析不兼容,因为带标签的小 DNA 和大 DNA 因 CUT&Tag 测定法结束时核膜遭打破开放而同时存在于样品中。带标签的 DNA 在 DNA 文库 PCR 扩增期间选择性富集,这有效稀释基因组 DNA 并使 CUT&Tag DNA 文库可用于 qPCR 分析。用 qPCR 产生优良信噪比是您还将能够成功对 CUT&Tag DNA 文库测序的强力指标。
CUT&Tag DNA 文库生成信噪比高得多的 qPCR 数据
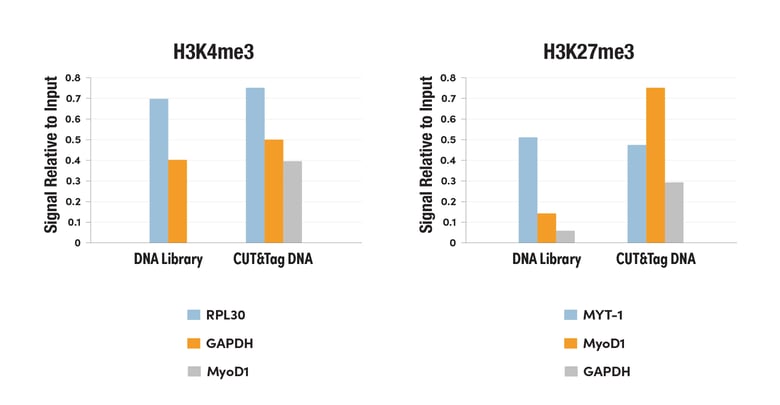
图 2. 使用 CUT&Tag Assay Kit #77552,对 HeLa 细胞和 Tri-Methyl-Histone H3 (Lys4) (C42D8) Rabbit mAb #9751进行 CUT&Tag。使用 CUT&Tag Dual Index Primers and PCR Master Mix for Illumina Systems #47415 制备 DNA 文库。 使用针对 H3K4me3、SimpleChIP® Human RPL30 Exon 3 Primers #7014 和 人 GAPDH 外显子 1 引物 Exon 1 Primers 的已知结合位点的阳性引物组,以及针对 H3K4me3、SimpleChIP Human MyoD1 Exon 1 Primers #4490 的已知阴性位点的阴性引物组,通过实时 PCR 对富集的 DNA 定量。每份样品中免疫沉淀的 DNA 的量表现为相对于染色质输入总量(其等同于一)的信号。
底线,不要让 Bioanalyzer 或 TapeStation 系统的低信号阻止您对 CUT&Tag 文库 DNA 测序。您可能会错过高质量结果。
参考
-
Kaya-Okur HS, Wu SJ, Codomo CA 等人 CUT&Tag for efficient epigenomic profiling of small samples and single cells. Nat Commun. 2019;10(1):1930. 发布于 2019 年 4 月 29 日。doi:10.1038/s41467-019-09982-5
C-03854


 沪公网安备31011502018823号
沪公网安备31011502018823号