CST® CAR Linker 抗体荣获 2023 年 CiteAb 颁发的创新奖。继续阅读了解详情!
—
嵌合抗原受体 (CAR) T 细胞疗法是一种革命性且快速演进的过继细胞免疫疗法,在利用身体自身免疫系统指导抗肿瘤应答方面显示出巨大前景。随着新 CAR-T 疗法的开发,用于表征表面表达 CAR 的检测试剂将对验证和优化新治疗方案至关重要。
然而,由于新 CAR 针对新肿瘤抗原设计,因此必须为每次迭代开发和验证独特的检测试剂,以确信 CAR 表面表达。这个过程不仅昂贵且耗时,而且伴随非特异性检测的问题可能导致进一步延迟。
但是,如果有一种通用检测试剂可以识别和确认您的 CAR 存在,而不管其抗原特异性,则情况如何?CST 开发了一组检测试剂,旨在识别工程免疫细胞上的多种 CAR:抗 CAR 接头抗体。
这些首次上市的试剂可以整合到多参数流式细胞术检测组合中,用于监测临床前模型中 CAR 的表达、转运和持久性。
当前方法:使用流式细胞术检测 CAR 表面表达
要了解这种新颖的 CAR 检测技术如何工作,让我们首先探索 CAR-T 细胞的结构和功能。
CAR 是旨在调节 T 细胞应答并将其重定向至自身起源性肿瘤抗原的工程化受体。顾名思义,该受体是一种可分解为四个主要组分的嵌合蛋白:胞外靶抗原结合结构域(例如,单链可变片段或 scFv)、间隔区或铰链结构域、跨膜结构域和至少一个胞内信号转导结构域(图 1)。这些元件的成功组合使 CAR-T 细胞重新定向,以辨识选定的抗原并杀伤肿瘤细胞。1
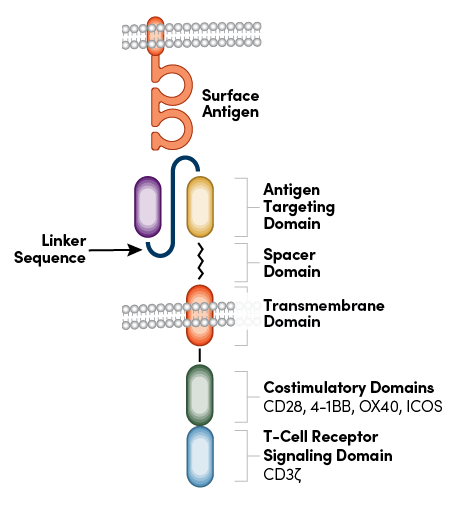 图 1:包含抗原靶向结构域和接头序列的 CAR 结构。
图 1:包含抗原靶向结构域和接头序列的 CAR 结构。
在发现和临床前研究期间设计 CAR-T 细胞时,科学家需要通过流式细胞术监测 CAR 表面表达,从而在某种程度上验证这些细胞的功能性。
大多数现有检测方法依赖结合于 CAR 细胞外结构域并利用 scFv 或铰链区可变重结构域或可变轻结构域内部特定序列的试剂。
根据所用 CAR-T 检测试剂的类别,可提供的解决方案往往缺乏特异性,可能不易整合到流式细胞术检测组合中,或者仅用于检测单一 CAR。
什么是抗 CAR 接头抗体以及它们如何起作用?
新型 CST 抗 CAR 接头抗体并不靶向可变重链结构域和可变轻链结构域或铰链区内部的序列,代之以靶向在 scFv 的可变重链结构域和可变轻链结构域之间的接头序列。由于大多数基于 scFv 的 CAR 包含重复性甘氨酸-丝氨酸接头序列(G4S 接头)或 Whitlow 接头2,所以抗 G4S 抗体和抗 Whitlow 抗体可用于使用流式细胞术监测几乎任何基于 scFv 的 CAR 的表面表达(图 2)。
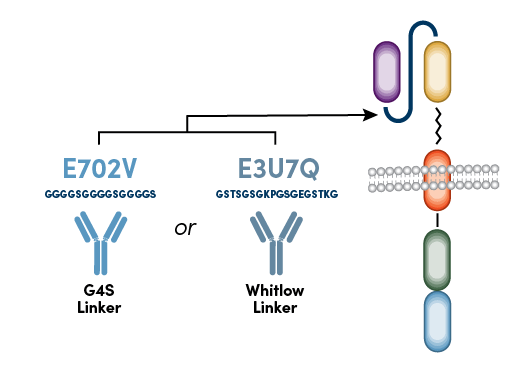
图 2. CST 抗 CAR 接头抗体识别 G4S 接头序列或 Whitlow 接头序列。
这适用于任何含有这些接头序列的 CAR ,包括靶向 CD19 抗原和 CD20 抗原的那些 CAR,这两种抗原是 B 细胞恶性肿瘤中高度表达的细胞表面分子。
 使用 G4S Linker (E7O2V) Rabbit mAb (PE Conjugate) #38907(右图)或浓度匹配的 Rabbit (DA1E) mAB IgG XP Isotype Control PE Conjugate #5742(左图)对从人 PBMC 分离并经过工程改造用于表达含有 G4S 连接蛋白的基于 scFv 的抗 CD20 CAR 的活性泛 CD3+ T 细胞进行流式细胞分析。Tag Blue 荧光蛋白 (TagBFP) 与 CAR 共表达。数据由匹兹堡大学 Lohmueller 实验室的 Michael Kirk 提供。
使用 G4S Linker (E7O2V) Rabbit mAb (PE Conjugate) #38907(右图)或浓度匹配的 Rabbit (DA1E) mAB IgG XP Isotype Control PE Conjugate #5742(左图)对从人 PBMC 分离并经过工程改造用于表达含有 G4S 连接蛋白的基于 scFv 的抗 CD20 CAR 的活性泛 CD3+ T 细胞进行流式细胞分析。Tag Blue 荧光蛋白 (TagBFP) 与 CAR 共表达。数据由匹兹堡大学 Lohmueller 实验室的 Michael Kirk 提供。
与所有 CST 产品一样,这些抗体均已使用我们针对特定应用的抗体验证方法并遵循抗体验证标志方法进行了严格验证。这包括在相关模型系统上进行测试,其中包括表达针对不同肿瘤抗原的 CAR 的原代人 T 细胞。这些抗体可按三种不同偶联物提供,并且还可以使用我们的定制偶联服务作定制偶联。
 结果就是一种经验证的通用 CAR 检测试剂,它可以通过消除不必要且耗时的步骤,加快您的发现研究或药物开发过程。
结果就是一种经验证的通用 CAR 检测试剂,它可以通过消除不必要且耗时的步骤,加快您的发现研究或药物开发过程。
下表显示了一些抗 CAR 接头抗体偶联物和制剂,但还有更多产品在不断增加。有关持续更新的列表,请参阅我们的产品目录,该目录现在包括 CAR 接头匹配的抗体对、细胞富集试剂盒等。此外,您还可以找到用于 CAR-T 细胞表型分析的荧光染料偶联抗体和用于分析组织中 CAR 靶标的多种经 IHC 验证的单克隆抗体。
CAR-T 疗法的快速发现和开发
长期以来,利用人体自身的免疫系统进行抗癌治疗一直是癌症研究者的梦想,而这一梦想通过 CAR-T 疗法成为了现实。已证明采用被称为“活药物”的 CAR-T 疗法,在单次输注后,能够持续数十年发挥疗效。
“[这种]创新性新产品[CST 抗接头抗体]有可能对癌症患者产生深远的影响,有助于开发和优化新疗法。”~ CiteAb 2023 年创新奖
这些用于治疗血液系统恶性肿瘤的革命性疗法的成功为开发新疗法铺平了道路,最显著的是实体瘤和衰老疾病,例如纤维化肝病和糖尿病。3-5 由于这种有前景的治疗方法将继续处于免疫疗法的前沿,目前正在开发的新疗法无疑将成为游戏规则改变者,为选择有限、难以治愈的癌症患者带来福音。
了解更多:
- 博客:利用 T 细胞快速活化和扩充过程加快免疫肿瘤学研究
- 详细了解我们的 CAR-T 疗法研究工具。
- 探索 CAR 信号转导网络互动通路。
- 观看 CAR-T 视频系列,以了解关于如何对 CAR-T 细胞工程化的更多信息并探索当前的研究挑战。
选择参考文献:
- Labanieh L, Majzner RG, Mackall CL. Programming CAR-T cells to kill cancer. Nat Biomed Eng. 2018;2(6):377-391. doi:10.1038/s41551-018-0235-9
- Whitlow M, Bell BA, Feng SL, et al. An improved linker for single-chain Fv with reduced aggregation and enhanced proteolytic stability. Protein Eng. 1993;6(8):989-995. doi:10.1093/protein/6.8.989
- Mohanty R, Chowdhury CR, Arega S, Sen P, Ganguly P, Ganguly N. CAR T cell therapy: A new era for cancer treatment (Review). Oncol Rep。2019;42(6):2183-2195. doi:10.3892/or.2019.7335
- Li JH, Chen YY. A Fresh Approach to Targeting Aging Cells: CAR-T Cells Enhance Senolytic Specificity. Cell. 2020;27(2):192-194. doi:10.1016/j.stem.2020.07.010
- Tenspolde, M., Zimmermann, K., Weber, L. C., Hapke, M., Lieber, M., Dywicki, J., Frenzel, A., Hust, M., Galla, M., Buitrago-Molina, L. E., Manns, M. P., Jaeckel, E., & Hardtke-Wolenski, M. (2019). Regulatory T cells engineered with a novel insulin-specific chimeric antigen receptor as a candidate immunotherapy for type 1 diabetes. Journal of Autoimmun. 2019;103:102289. doi:10.1016/j.jaut.2019.05.017
CST 和 Cell Signaling Technology 是 Cell Signaling Technology, Inc. 的商标或注册商标。Alexa Fluor 是 Life Technologies 公司的注册商标。所有其他商标均属各自所有者专有。访问 cellsignal.com/trademarks 了解更多信息。22-BPA-10837


 沪公网安备31011502018823号
沪公网安备31011502018823号