大约八分之一的男性在其一生中会被诊断出患有前列腺癌,这使其成为美国男性癌症相关死亡的第二大原因。1,2早期前列腺癌的生长通常是雄激素依赖性的,因此对激素疗法反应良好。
那么,为什么这么多男性在与这种普遍存在的癌症的斗争中失败了呢?在许多晚期前列腺癌病例中,例如去势抵抗性前列腺癌 (CRPC),该疾病变得不依赖雄激素并且不再对激素疗法有反应。因此,早期发现对于改善生存结果至关重要。前列腺特异性抗原 (PSA) 的常规血液检测用于识别可能需要进一步诊断评估的男性。
这篇文章回顾了一些当前和新兴的 CRPC 治疗策略。
前列腺癌治疗的当前和未来方向
目前,对抗 CRPC 的第一道防线包括阿比特龙(一种减少雄激素产生的雄激素生物合成抑制剂)和恩杂鲁胺(一种雄激素受体 (AR) 拮抗剂)。然而,许多癌细胞最终会对这些治疗产生抗药性。
因此,开发新的治疗方法或联合疗法对于改善晚期前列腺癌患者的治疗效果至关重要。
受关注的基因突变和变异
前列腺癌中的几种基因突变已被确定为可能的治疗靶点,包括 50% 前列腺癌中存在的 TMPRSS2-ERG 融合蛋白。其他经常观察到的基因改变包括 ERG、TMPRSS2、CHD1、FoxA1、SPOP 和 BRCA1/2 突变。
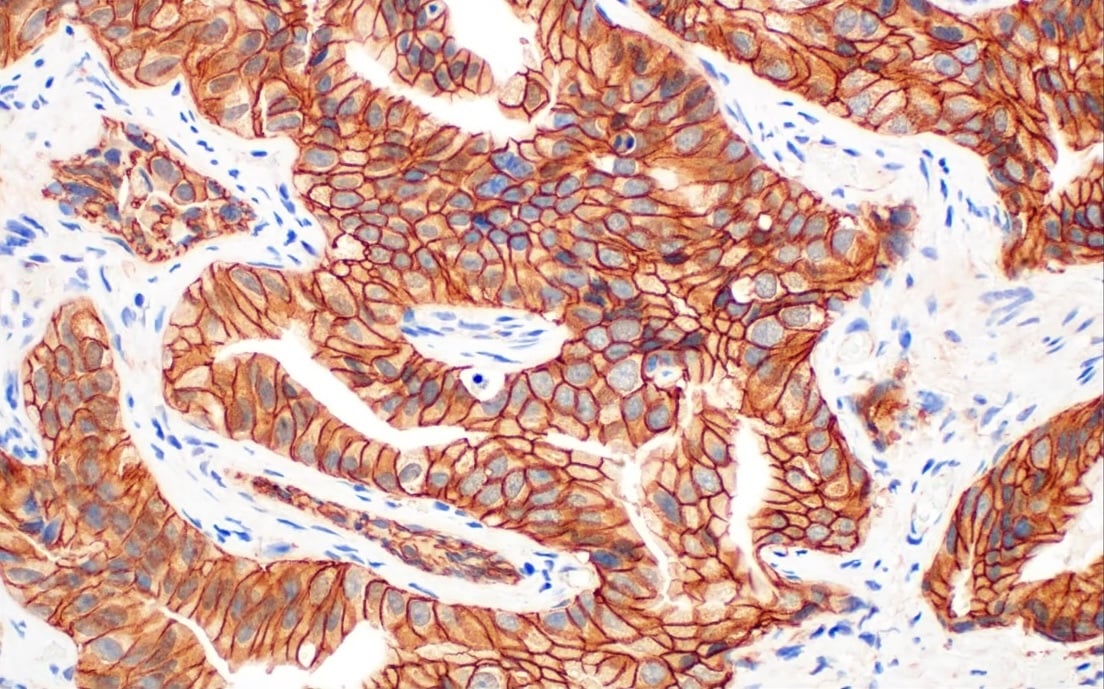
 使用 ERG (A7L1G) Rabbit mAb #97249 对石蜡包埋的人前列腺癌组织(两个不同病例)进行免疫组织化学分析。
使用 ERG (A7L1G) Rabbit mAb #97249 对石蜡包埋的人前列腺癌组织(两个不同病例)进行免疫组织化学分析。
此外,AR-V7 和 ARv567 等 AR 变体也继续引起人们的兴趣。这些变体往往通过异常剪接产生,并且缺乏配体结合域,从而导致前列腺癌细胞的雄激素非依赖性生长。这使得肿瘤细胞具有持续增殖的能力,这是癌症的标志之一。AR-V7 是 CRPC 的关键驱动因素,在转移性和 CRPC 中高度表达。因此,人们正在探索旨在控制导致不同变异出现的剪接事件的治疗方法,以及针对特定变异的治疗方法。3,4
联合治疗策略
一种组合方法是针对表观遗传机制和免疫疗法来解决肿瘤避免免疫破坏的能力,这是另一个癌症标志。5 单独使用免疫疗法治疗患者通常无效,因为前列腺癌往往缺乏 T 细胞浸润,因此被认为是免疫学上的“冷”细胞。然而,EZH2 抑制剂在治疗恩杂鲁胺治疗后发生的 CRPC 和神经内分泌前列腺癌方面已显示出良好的前景。EZH2 是一种调节染色质以沉默基因功能的甲基转移酶,并且在 CRPC 中高度表达。研究表明,EZH2 抑制剂可以通过重新激活 STING 通路来触发前列腺癌的“冷”开关,使其对免疫疗法更敏感。
PARP 抑制剂,包括奥拉帕尼和鲁卡帕尼,可能在 CRPC 患者的个体化医疗治疗中发挥作用,尤其是对于同源重组修复通路发生突变的患者,大约 30% 的患者存在这种突变。然而,一般 PARP 抑制的总体功效仍有待确定。6,7
紫杉烷是一种标准的化疗药物,可与雄激素信号转导抑制剂(如阿比特龙或恩杂鲁胺)联合使用。在一项研究中,使用卡巴他赛和雄激素信号抑制剂治疗之前接受过多西他赛和 AR 抑制剂治疗的患者,临床结果得到改善。8,9
早期发现阶段有前景的治疗方法包括:
- 降解 SWI/SNF 的组分,SWI/SNF 是一种染色质重构复合体,可促进转录因子进入增强子元件,从而增加 FoxA1 和 ERG 的表达。
- 截至 2022 年 2 月,研究人员还开发了一种药物,目前已进入 1A 期临床试验,该药物可以恢复抑制雄激素受体表达的长链非编码 RNA。
- 最后,科学家正在攻击导致 AR 抑制剂疗法产生耐药性的机制。前列腺癌细胞的糖皮质激素受体表达增加,该受体与雄激素受体有相似之处,当 AR 信号受到抑制时,它会进行补偿。10当糖皮质激素受体受到抑制时,肿瘤会恢复对一线治疗方案的反应性。
前列腺癌治疗的未来
去势抵抗性前列腺癌的预后仍然具有挑战性,但对新型联合疗法的持续评估为改善患者的治疗效果带来了希望。探索有效联合治疗的研究只会为临床医生提供更大的资源库,用于对抗去势抵抗性前列腺癌,最终挽救生命。
参考文献
- American Cancer Society – Key Statistics for Prostate Cancer
- National Cancer Institute – Prostate Cancer
- Liu LL, Xie N, Sun S, Plymate S, Mostaghel E, Dong X. Mechanisms of the androgen receptor splicing in prostate cancer cells. Oncogene. 2014;33(24):3140-3150. doi:10.1038/onc.2013.284
- Takayama KI. Splicing Factors Have an Essential Role in Prostate Cancer Progression and Androgen Receptor Signaling. Biomolecules. 2019;9(4):131. Published 2019 Apr 1. doi:10.3390/biom9040131
- Morel KL, Sheahan AV, Burkhart DL, et al. EZH2 inhibition activates a dsRNA-STING-interferon stress axis that potentiates response to PD-1 checkpoint blockade in prostate cancer. Nat Cancer. 2021;2(4):444-456. doi:10.1038/s43018-021-00185-w
- McFarland TR, Kessel A, Swami U, Agarwal N. Development of PARP inhibitor combinations for castration resistant prostate cancer unselected for homologous recombination repair mutations. Am J Transl Res. 2021;13(7):7427-7439. Published 2021 Jul 15.
- Antonarakis ES, Gomella LG, Petrylak DP. When and How to Use PARP Inhibitors in Prostate Cancer: A Systematic Review of the Literature with an Update on On-Going Trials. Eur Urol Oncol. 2020;3(5):594-611. doi:10.1016/j.euo.2020.07.005
- de Wit R, de Bono J, Sternberg CN, et al. Cabazitaxel versus Abiraterone or Enzalutamide in Metastatic Prostate Cancer. N Engl J Med. 2019;381(26):2506-2518. doi:10.1056/NEJMoa1911206
- Zhang PF, Xie D, Li Q. Cost-effectiveness analysis of cabazitaxel for metastatic castration resistant prostate cancer after docetaxel and androgen-signaling-targeted inhibitor resistance. BMC Cancer. 2021;21(1):35. Published 2021 Jan 7. doi:10.1186/s12885-020-07754-9
- Shah N, Wang P, Wongvipat J, et al. Regulation of the glucocorticoid receptor via a BET-dependent enhancer drives antiandrogen resistance in prostate cancer. Elife. 2017;6:e27861. Published 2017 Sep 11. doi:10.7554/eLife.27861


 沪公网安备31011502018823号
沪公网安备31011502018823号