在设计实验和生成可重复数据时,了解抗体的制备方式以及不同类型抗体的优缺点至关重要。在 Antibody Essentials 系列内容第 1 部分,我们讨论了抗体如何产生、它们的结构和功能以及抗体其他基础知识。在这里,我们将了解带给抗体难以置信的功能多样性的生物学机制,并考虑抗体可以分类的各种方式。
目录
了解抗体多样性和分类
如您所知,抗体是一种复杂的蛋白质,由特定类别的免疫细胞(称为 B 细胞)在获得性免疫反应过程中产生。免疫系统需要能够识别在动物的一生中可能遇到的数千种不同的潜在病原体,但抗原数量几乎无限,那 B 细胞如何产生针对所有这些潜在目标的抗体?为了解决这个问题,让我们简要探讨一下 B 细胞如何发育的一些基础知识,以了解它们在免疫学中的作用。
如何产生抗体多样性?
在骨髓和脾脏中成熟后,每个循环型 B 细胞都表达一种独特的 B 细胞受体 (BCR),该受体由膜免疫球蛋白(抗体)和相关的 Igα/Ig (CD79a/CD79b) 异二聚体组成。当 BCR 遇到并识别抗原时,B 细胞会内化并处理抗原。抗原片段与主要组织相容性复合体 (MHC) II 类分子结合以形成复合体,而这种片段-MHC II 类复合体最终展示在 B 细胞表面上。T 辅助 (Th) 细胞上的受体识别该复合体并结合之,从而使 Th 细胞活化,这转而产生使 B 细胞活化以变成增殖性 B 浆细胞的细胞因子。这导致一群相同的、分泌抗体的浆细胞快速克隆扩增,这些浆细胞招募免疫细胞来杀死病原体并促进免疫系统清除抗原。尽管许多浆细胞寿命很短,但仍有一部分存活下来成为记忆 B 细胞,在随后接触相同抗原时发挥保护功能。
获得性免疫的有效性取决于每个 B 细胞克隆在其表面表达不同的抗体这一事实。那么,它来自哪里呢?
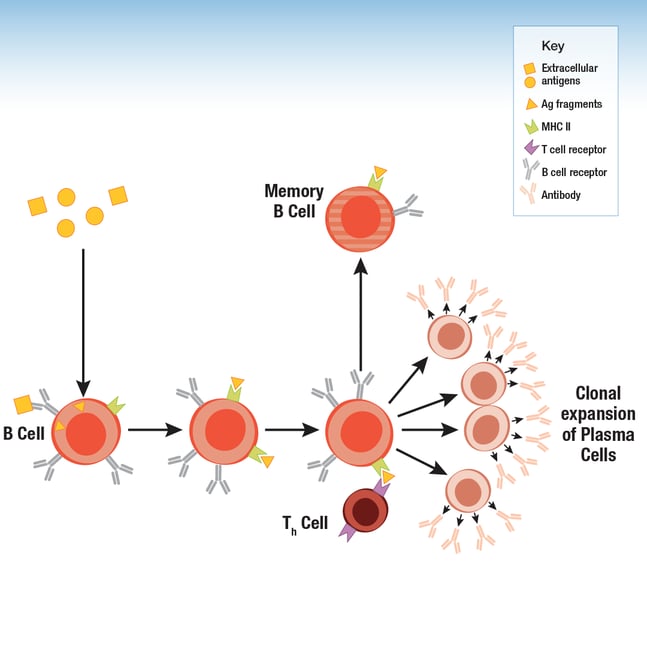 图 1. B 细胞通过表面的 MHC II 复合物显示抗原片段。 在免疫应答期间,Th细胞会刺激 B 细胞的克隆扩增,从而推动抗体产量的增加。
图 1. B 细胞通过表面的 MHC II 复合物显示抗原片段。 在免疫应答期间,Th细胞会刺激 B 细胞的克隆扩增,从而推动抗体产量的增加。
B 细胞表面的抗体多样性是在 B 细胞发育早期、成熟之前通过一个过程实现的,该过程包括编码抗体重链和轻链的基因的 DNA 重排。这是通过三个主要机制发生的:V(D)J 重组、连接多样化和体细胞突变(图 2)。
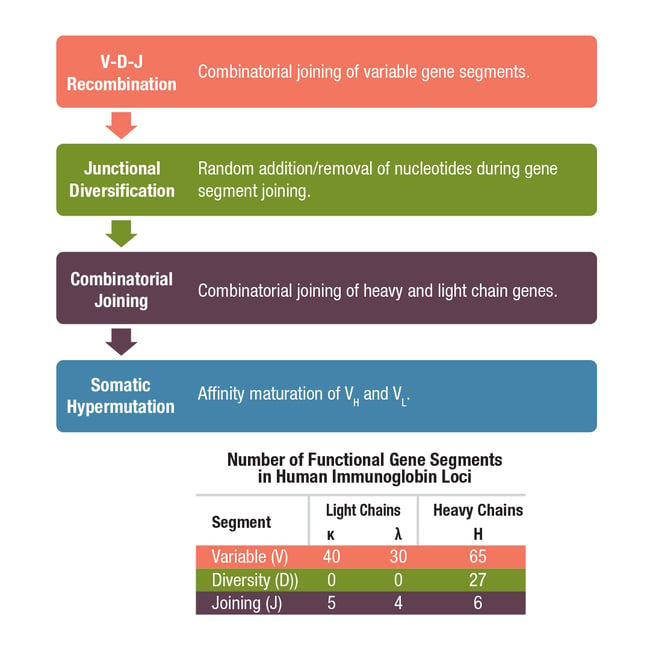
图 2. 参与抗体多样性产生的机制。
首先让我们来看一下 V(D)J 重组,这是 B 细胞发育期间不同可变基因节段、多样性基因节段和连接基因节段的剪切过程。每条抗体重链因单一恒定链基因剪切成一个可变基因节段、一个多样性基因节段和一个连接基因节段产生,而轻链由 V 节段(kappa/κ 或 lambda/λ)和 J 节段组成,但不包括 D 节段。庞大数目的可用 V、D 和 J 基因节段(图 2)连同淋巴细胞特异性重组酶复合体所致的节段随机重组产生数百万种可能的基因构型。这种多样性为连接多样化进一步增加,即 V(D)J 酶复合体连接 V 区编码序列时,从 V 区编码序列末端丢失或在其末端添加随机核苷酸。
一旦 V(D)J 重组和连接多样化完成,重链基因序列和轻链基因序列以正确顺序排列以产生有功能的抗体多肽。然而,基因重组受第三层面的多样化(称为体细胞突变)影响。体细胞超突变涉及重链和轻链可变区中点突变的积累,并在 B 细胞活化后发生。这些突变率比其他基因的背景突变率高约一百万倍,以进一步使抗体库多样化。随着适应性免疫应答推进,这产生亲和力更高的抗体,一个称为亲和力成熟的过程。总之,这些多样化机制允许产生能够响应数十亿种独特抗原的抗体,足以确保对任何非自身抗原产生免疫应答。
进一步阅读:Janeway CA Jr, Travers P, Walport M, et al.The generation of diversity in immunoglobulins. 免疫生物学:The Immune System in Health and Disease. 5th edition. New York: Garland Science; 2001.
抗体如何分类?
我们已经考虑完抗体多样性背后的机制,是时候考虑抗体分类了。抗体通常以多种方式分类,包括:
- 靶标反应性
- 物种反应性
- 用于免疫/抗体生产的宿主物种
- 多克隆或单克隆
- 仅限研究用途、诊断用途或治疗用途
- 重组或非重组抗体生产
下面,我们将更详细地逐一探讨这些抗体分类范畴。
靶标反应性
当您开始选择实验中使用的抗体时,您首先可能想到靶标反应性。既有特异性又有选择性的充分表征的抗体将与其靶标生物分子(最常见为蛋白质)反应并结合,并且不与脱靶分子反应。靶标蛋白的名称通常包含在抗体产品的名称中,以提示预期的靶标反应性。
对于许多靶标,将可提供不止一种与靶标反应的抗体,这些抗体可能识别同一靶标的不同表位,并且性能特征略有不同。因此,设计实验时钻研验证数据并更详细了解每条数据至关重要。
使用得当时,具有特异性但选择性较弱的抗体可能仍然是有价值的工具。一个例子是这种泛钙粘蛋白抗体,它与钙粘蛋白家族多个成员中表达的保守抗原反应。使用泛特异性抗体的筛选实验可以继而使用选择性更强的抗体锁定该家族内部各个靶标。
作为正常或病理生物过程中细胞信号活动的结果,许多蛋白质经历翻译后修饰 (PTM),例如磷酸化、剪切、甲基化、泛素化或乙酰化。PTM 可以激活或制止蛋白质的信号转导或其他功能。修饰特异性抗体,顾名思义,将与在特定氨基酸残基处携带特定类型修饰的靶标反应,而不与未修饰的靶标反应。可能有用的是,设计包含修饰特异性抗体和识别总(修饰 + 未修饰)表达水平目标蛋白的另一种抗体的实验,旨在确认已修饰抗体读出结果的变化是激活状态变化的结果而不是目标表达的变化(图 3)。
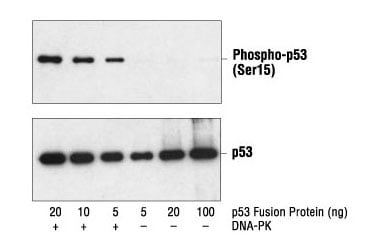 图 3. 使用 Phospho-p53 (Ser15) Antibody #9284(上图)和 p53 Antibody #9282(下图)对未经处理或通过 DNA-PK 磷酸化的 p53 融合蛋白进行蛋白质印迹分析。
图 3. 使用 Phospho-p53 (Ser15) Antibody #9284(上图)和 p53 Antibody #9282(下图)对未经处理或通过 DNA-PK 磷酸化的 p53 融合蛋白进行蛋白质印迹分析。
其他抗体已经开发出来,具有针对点突变和其他类型突变的特异性。点突变特异性抗体只会与带有特定氨基酸取代的靶标蛋白发生反应。融合特异性抗体仅识别由框内融合突变产生的蛋白质,例如 SS18-SSX 融合蛋白,不太常见。截断突变可以通过设计实验来探测,这些实验结合了识别截短蛋白质的 N 端和 C 端的抗体。识别癌症等疾病过程中涉及的突变的抗体可能会继续开发为临床诊断工具(见下文)。
物种反应性
不要与下一段中描述的抗体宿主物种混淆,物种反应性指靶标蛋白的物种。例如,许多在小鼠中表达的蛋白质将具有在其他哺乳动物物种中表达的同源物或进化上相关的蛋白质。在某些情况下,针对小鼠抗原产生的抗体只会与小鼠同源物反应,而不会与该蛋白质的人类或大鼠同源物反应。其他抗体将能够与来自多个物种的同源物反应。抗体是否具有广泛或狭窄的物种反应性主要受表位中序列保守程度的影响;高度保守的表位更可能产生可以针对多个物种中靶标加以验证的抗体。
您将需要选择一种其物种反应性适合您手头实验模型的抗体。因此,对于采用小鼠细胞系的实验,您会盼望小鼠物种反应性,但如果使用人类细胞系,您会盼望人类的反应性。在外源性表达模型情况下,例如小鼠细胞系中表达人类蛋白质,您需要选择具有人类反应性且另外对小鼠同源物不反应的抗体,不过也可能进行替代性实验设计,如敲除小鼠同源物或将表位标签工程化入外源表达的蛋白质中。
抗体宿主物种
抗体也可以根据产生它们的物种进行分类。兔、小鼠和大鼠是最常用于产生研究用抗体的宿主物种,单克隆抗体情况下尤其如此。这部分是因为这些物种的畜牧业相对简单。尽管多克隆抗体可以在小鼠或大鼠中产生,但它们通常产自从中更易采集大量血清的体型较大动物,例如兔、山羊、驴或绵羊。
一种常见的多重免疫测定方法将针对不同目标的一抗(分别来自不同宿主物种)与偶联于不同荧光团的二抗组合。在此实验设计中,根据一抗中恒定区的物种特异性,每种二抗将仅识别一种一抗。
例如,“山羊抗小鼠 IgG”二抗在山羊宿主中产生并且将识别小鼠宿主产生的一抗。与荧光染料的偶联使得在显微镜、流式细胞仪或其他仪器中检测和读出每个靶标成为可能。然而,跟踪关键细节(例如宿主物种和同种型)至关重要,并且所有一抗和二抗都必须针对其预期用途进行充分验证。否则,将获得误导性的结果。
抗体同种型和亚类
在哺乳动物中,抗体根据其包含的重链划分成五个主要同种型或类别。这些类别称为 IgG、IgA、IgD、IgE 和 IgM,其中重链分别是 γ、α、δ、ε 或 μ。各重链就恒定域数目和序列及铰链区结构而言相异,并且在某些物种中允许将每个抗体同种型进一步划分为亚型(图 4)。
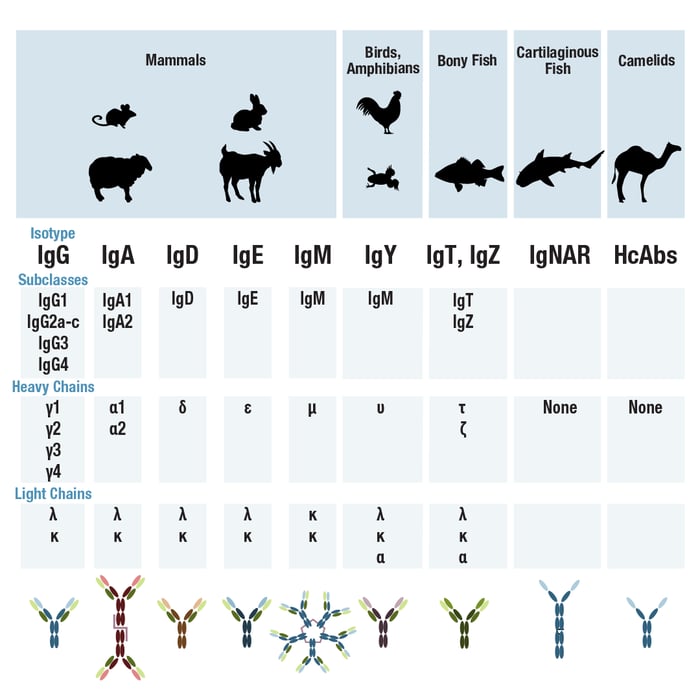
例如,在人类中,IgG 同种型分为四个亚型或亚类(IgG1 到 IgG4),而在小鼠中存在五个不同的 IgG 亚型。兔子只有一种同种型:IgG. 具有不同靶点特异性但具有相同亚型的抗体在其恒定域中将具有相同的序列。因此,如果被胃蛋白酶切割,它们将产生相同的 Fc 片段。也有可能针对同一抗原产生来自不同物种、同种型或亚型的两种或多种抗体。
通过在同一实验中组合不同同种型或亚型的抗体,可以给多重实验设计增加另一层复杂性。例如,可以区分小鼠 IgG1 与小鼠 IgG2a 的亚类特异性二抗将与来自这些亚类的一抗组合。
值得一提的是,在所有哺乳动物中,根据 B 细胞成熟期间选定的轻链基因座,抗体轻链划分为 κ 或 λ。轻链类型是另一种可用于实现多重分析的抗体特性。同样至关重要的是指出,非哺乳动物物种具有异于哺乳动物的抗体同种型。例如,鸟类产生 IgY 抗体,而硬骨鱼类(如虹鳟)产生 IgT。同样,检测不同同种型依赖于可获得合适的、经彻底验证的二抗试剂。
最后,抗体同种型之间的另一个主要差异是抗体亲和力或抗体价数,即可用抗原结合位点数目。例如,虽然 IgG、IgD 和 IgE 为二价,但 IgA 具有价数 4 而 IgM 具有价数 10。正如我们在第一篇 Antibody Essentials 博客中看到以及图 5 中再次说明,价数越大,免疫球蛋白分子可以结合的抗原越多,其亲和力就越高。
克隆性:多克隆与单克隆抗体
另一种对抗体进行分类的方法是考虑它们是多克隆还是单克隆;两者之间的主要区别是指产生它们的 B 细胞。多克隆抗体衍生自混合的或异质 B 细胞群,这意味着一管多克隆抗体实际上将包含许多不同的抗体。如果多克隆抗体具有高度选择性,则该混合物中的抗体将于结合靶标蛋白内部的多个表位,但不结合任何其他表位(图 5)。
另一方面,单克隆抗体由相同的 B 细胞产生,因此一管纯化的单克隆抗体将包含同一抗体的多个副本并且应该结合于单一表位。最重要的是,如果可用,单克隆抗体比多克隆抗体提供更一致的性能,这一主题将在 Antibody Essentials 系列的第 4 部分中进行更详细的探讨。
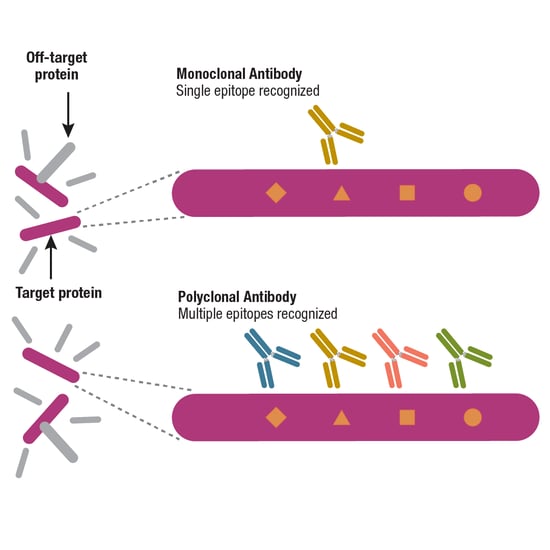
图 5. 经充分验证的单克隆抗体应特异性识别单一表位,而经充分验证且具有选择性的多克隆抗体仍应结合于单一靶标蛋白结合,但通过识别多个表位来实现。
重组抗体
另一种进一步划分单克隆抗体的方法是考虑它们是否使用传统方法或重组方法生产。更准确地说,让我们考虑重组单克隆抗体生成和生产之间的差异。
您可能已经阅读过关于使用噬菌体和酵母展示文库作为高通量抗体发现的无动物环境。这可以被认为是重组抗体的产生。请注意,重组单克隆抗体生产不完全限于已体外生成的抗体。也可以始于常规免疫接种动物以激发免疫应答和 B 细胞扩充,生产重组抗体。在成熟 B 细胞的分离和克隆扩增(在 Antibody Essentials 的第 4 部分中介绍)之后,重链和轻链的基因被克隆和测序。这是重组抗体的显著特征:它的基因和肽序列为开发它的科学家所知,从而能够在细胞培养中表达抗体以进行放大生产。重组单克隆抗体生产往往是许多研究应用的首选项,提供持续的抗体供应,并且更重要的是,对于最终用户,它们具有更高的批间一致性和可靠性能。
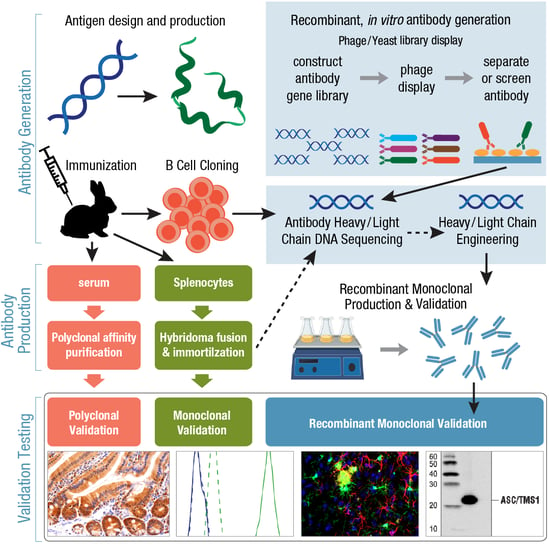
图 6. 多克隆、单克隆或重组单克隆抗体的抗体生成、生产和验证工作流程概述。
由于它们经过测序并适合工程化,因此重组抗体作为治疗剂的使用正在增加,主要例子是抗体-药物偶联物的开发。其他治疗方法包括在动物宿主物种中开发的物种转换或人源化抗体,以降低免疫原性和人类抗小鼠抗体 (HAMA) 反应; 生产单链可变片段以保持特异性,同时显著降低抗体大小; 以及能够同时结合两个不同表位的双特异性抗体的产生。
仅供研究使用 (RUO) 的抗体
一个重要的抗体分类涉及使用抗体的环境。如果您在学术研究实验室工作,您很可能使用标有“仅供研究使用”(有时缩写为 RUO)的抗体。与下面介绍的治疗性抗体相反,ROU 抗体预期用于非诊断性、基于实验室的实验(下图 6)。
根据目标的生物学作用以及对预期应用有意义的使用方法、实验步骤和对照材料行设计 RUO 抗体的验证测试。例如,被认为对蛋白质印迹有效的 RUO 抗体应提供其适用于蛋白质印迹应用的明确实验证明,数据显示其对阳性和阴性对照的性能。至关重要的是指出,一种应用中的验证并不意味着抗体必定会在其他应用中起作用。例如,蛋白质印迹验证数据并不保证抗体适用于免疫组织化学 (IHC) 或流式细胞术 (IF)。因此,寻找与您将会使用抗体的应用有关的验证数据至关重要。
进一步阅读:更多了解验证技术和抗体验证标志
与治疗性抗体相比,RUO 抗体通常不受严格监管,因此最终由研究人员决定从制造商可提供的抗体验证数据是否足够用。验证不当的抗体已经助长抗体可重复性危机,因此至关重要的是,确定您是否信任所用抗体以及您的实验数据是否足以发表结果。
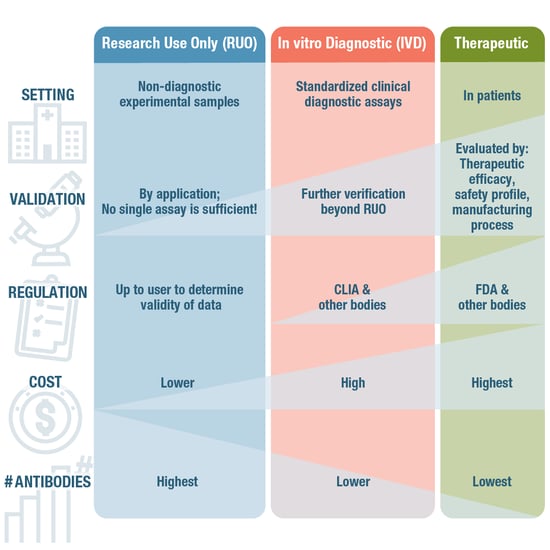
图 6. 与 RUO 抗体相比,用于诊断和治疗用途的抗体必须满足更严格的验证标准才能获得批准。
治疗性抗体
与 RUO 抗体相反,治疗性抗体旨在用于患者。治疗性抗体的特殊之处在于它们具有可用于治疗疾病的生物活性。治疗性抗体的作用机制可能是阻断配体-受体相互作用,中断信号级联反应,或用辐射或不同形式的细胞毒性靶向肿瘤细胞以杀死它们。这意味着它们需要一种迥然不同的确认或验证方法,如在这个领域更常提到那样。治疗性抗体不是仅依赖于特定应用的验证,而是通过其治疗功效、安全性和制造工艺进行评估,从而使用正式的工艺表征来确保临床试验中的患者安全。
在美国,这受到食品和药物管理局 (FDA) 等机构严格监管,FDA有权批准或拒绝治疗性抗体,就像对待任何其他药物一样。可以想象,开发 FDA 批准的疗法的成本远高于 RUO 抗体!
临床诊断抗体
位于 RUO 抗体和治疗性抗体之间的诊断抗体用于临床环境中患者来源的样本。在这里,它们是用于诊断病原体感染、癌症、代谢或免疫疾病以及许多其他医疗状况的标准化检测的重要工具。尽管一些免疫测定(包括 IHC 和 ELISA )可以并入 RUO 或诊断用途抗体,但临床诊断用途要求由管治机构(例如美国的临床实验室改进修正案 (CLIA))进行额外层级的验证和认证。
总结
归根结底,抗体的分类取决于其生产方法、内在特性及其适用的应用。在为您的检测选择最佳抗体并满足您的研究和发表目标时,应考虑所有这些因素。
接下来,我们将在“ Antibody Essentials 第 3 部分:抗体技术如何发展”中深入探讨抗体技术的历史和发展,以及它如何影响您目前抗体使用的决定。
阅读整个 Antibody Essentials 系列内容:
- Antibody Essentials 第 1 部分:抗体基础知识
- Antibody Essentials 第 2 部分:抗体多样性和分类
- Antibody Essentials 第 3 部分:抗体技术如何发展
- Antibody Essentials 第 4 部分:多克隆与单克隆抗体
- Antibody Essentials 第 5 部分:抗体选择的重要考虑因素
20-FLE-62535


 沪公网安备31011502018823号
沪公网安备31011502018823号