癌细胞抵制可能会阻止其生长的抑制信号。涉及的主要途径是自噬和死亡受体信号转导(细胞凋亡),这两种通路最终都可能导致细胞死亡和肿瘤生长减少。

自噬是一个动态细胞循环系统,可降解细胞浆内容物、异常蛋白聚合物以及多余或受损的细胞器,以便氨基酸等构建模块可用于生成新的细胞组分。因此,自噬是一个促进存活的过程。癌症可以上调自噬以在微环境压力下存活并增加生长和侵袭性。自噬过程涉及自噬体的形成,然后与溶酶体融合形成自噬溶酶体。该过程受 mTOR/AMPK/PI3K/MAPK 通路调控。
目标蛋白质:
- Atg16L1 在促进形成大复合物方面起着关键作用,然后需要这种复合物来形成自噬体,即将细胞质成分传递至溶酶体的结构。
- Sequestosome 1 (SQSTM1, p62) 是一种泛素结合蛋白,可与泛素相互作用并为多种信号转导蛋白提供支撑。它通过蛋白酶体或溶酶体触发蛋白质降解。
- 自噬标记轻链 3 (LC3) 与自噬囊泡相关。自噬体中存在 LC3,以及 LC3 向 LC3-II 的转化被视为发生自噬的“指示器”。
- Atg1/ULK1 可以用作控制自噬的多个信号的会聚点。
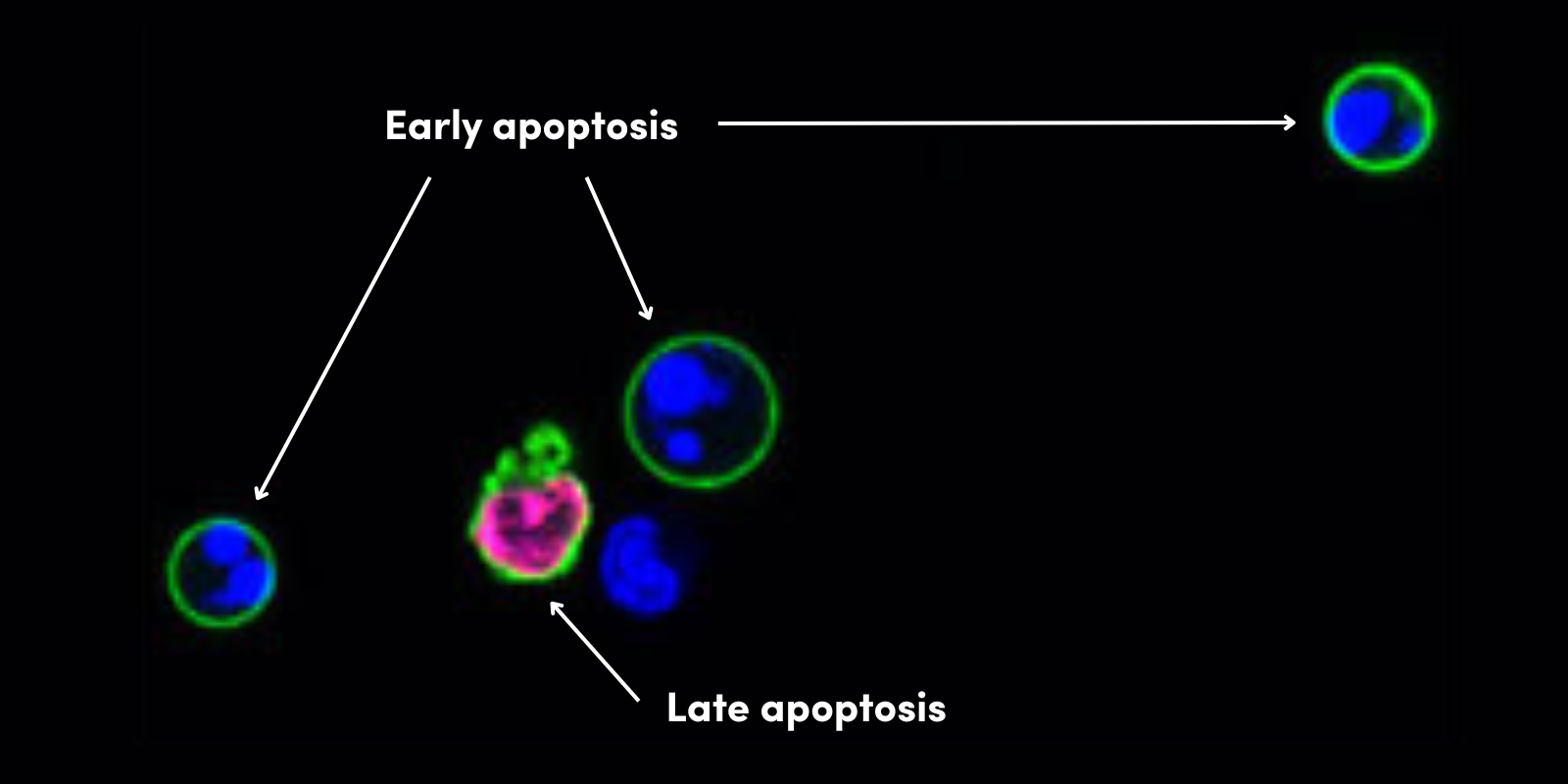
细胞凋亡(程序性细胞死亡)可以通过激活死亡受体来诱导。
目标蛋白质:
- Caspase-8: 通过激活 caspase-8 的几种受体诱导细胞凋亡,并导致 caspase-8 活性片段的释放,然后裂解并激活下游 caspase。
- RIP 激酶是重要的细胞应激调节分子,可通过 NF-κB 激活和促凋亡通路诱导促活和炎症反应。
- Bcl-2 通过抑制线粒体细胞色素 c 的释放而对一系列的凋亡刺激因素做出响应,从而发挥其促进存活的功能。
了解有关逃避生长抑制因子的通路和蛋白质的更多信息
查看肿瘤研究靶标标志的完整指南:
《癌症标志》是 Robert Weinberg 和 Douglas Hanahan 博士的开创性手稿,发表在《细胞》杂志上。1 作者提出了这样的想法,即可以将癌症的复杂性分解为基本原理的较小子集。这里的信息与一个癌症标志有关,称为“逃避生长抑制因子”。本系列中的其他条目探讨了其他提议的标志。
阅读癌症标志系列中的其他博客文章,了解更多信息:
选择参考文献:
- Hanahan D, Weinberg RA (January 2000). "The Hallmarks of Cancer". Cell. 100 (1): 57–70. doi:10.1016/S0092-8674(00)81683-9
- Hanahan D, Weinberg RA (March 2011). "Hallmarks of Cancer: the next generation". Cell. 144 (5):646-74. doi: 10.1016/j.cell.2011.02.013.


 沪公网安备31011502018823号
沪公网安备31011502018823号