我们对癌细胞了解的一点是:它们可以抵抗死亡。它们回避凋亡,一旦细胞受损,凋亡机制即会导致细胞死亡。通常,细胞凋亡有助于通过生长和发育保持生物体健康,并通过去除感染或受损的细胞来维持机体组织。但是,不管癌细胞生长有多异常,它们都不会遵循这一过程。

癌细胞可能会改变检测损伤或异常的机制,从而阻止适当的信号转导和凋亡激活。癌细胞也可能在下游信号转导中或凋亡相关蛋白中引入缺陷,这也将阻止正常的凋亡 1,2。
细胞凋亡在逃避生长抑制因子的标志中也很重要,但这是指由外部信号触发的细胞凋亡。当提到这个标志,我们指的是内在凋亡,其中凋亡程序从未开始。
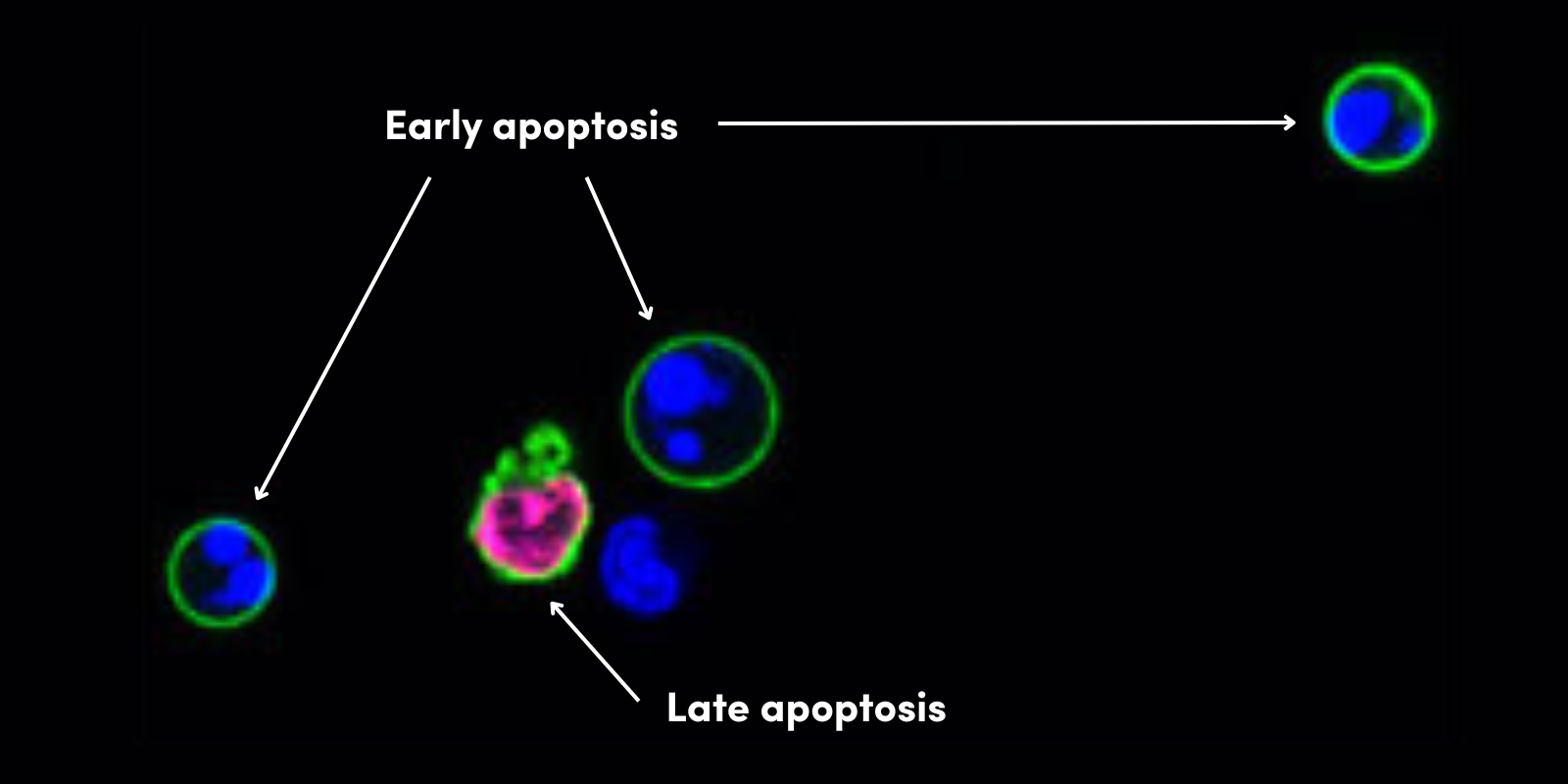
要发现癌细胞如何逃避细胞死亡,我们必须首先研究可能发生凋亡的不同途径。
通过激活死亡受体可以诱导细胞凋亡。
- Caspase-8 :通过激活 caspase-8 的几种受体诱导细胞凋亡,并导致 caspase-8 活性片段的释放,然后裂解并激活下游 caspase。
- RIP 激酶:(在该途径的受体附近)是细胞应激的重要调节剂,可通过激活 NF-kB 以及促凋亡途径来触发促生存和炎症反应。
- Bcl-2:通过抑制线粒体细胞色素 C 的释放而对一系列的凋亡刺激因素做出响应,从而发挥其促进存活的功能。
- p53: “主开关”是一种肿瘤抑制蛋白,在细胞应答 DNA 损伤和其他基因组畸变中起着重要的作用。p53 的激活可导致细胞周期停滞和 DNA 修复或凋亡。p53 可以被多个蛋白(包括 Chk2 和 ATM)在多个位点磷酸化和乙酰化。
《癌症标志》是 Robert Weinberg 和 Douglas Hanahan 博士的开创性手稿,发表在《细胞》杂志上。1 作者提出了这样的想法,即可以将癌症的复杂性分解为基本原理的较小子集。此处的信息与一个癌症标志有关,称为“抵抗细胞死亡”。本系列中的其他条目探讨了其他提议的标志。
其他资源



 沪公网安备31011502018823号
沪公网安备31011502018823号